化学で最重要~電気陰性度~
こんにちは、ナツキです!
今回は、
「電気陰性度」
について話していきます。
この「電気陰性度」、
名前はパっとしないですが、
間違いなく高校化学で
一番重要です。
理論、有機、無機
どの分野でもこれは
避けては通れません。
理解の面でもそうですが、
これを知っていると
「応用力」がつきます。
覚える量が
圧倒的に減ります。
暗記量を減らして、
覚えてる友達を横目に、
「それ覚える必要ないのにな~」
って思いたくないですか?
ちょっと考えただけなのに、
「そんなことまで知ってるんだ!」
なんて言われたりもします。
そうなるために、最低限、
・電気陰性度とは何か?
・強さの順序
は今回マスターしましょう。
「電気陰性度」は、
簡単に言うと、
共有電子対を
引っ張る力の強さです。
まず、「共有電子対」について、
説明します。
原子は結合するとき、
電子を一個ずつ出し合います。
その電子一個ずつを共有して
結合するので、
共有結合と呼ばれます。
そして、共有している2つの電子たちを、
「共有電子対」
といいます。
しかし、
一個ずつ出したからと言って、
それを等しく使えるわけでは
ありません。
取り合いが起こります。
例えば、
兄弟が1万円ずつだして
買ったとしましょう。

しかし、
やりたい時間が重なってしまうと、
取り合いになります。
いざ取り合いになるとしまうと、
どうでしょう?
大体の場合お兄ちゃんのほうが、
引っ張る力が強いので、
お兄ちゃんがたくさん使います。
この「引っ張る強さ」のことを、
「電気陰性度」といいます。
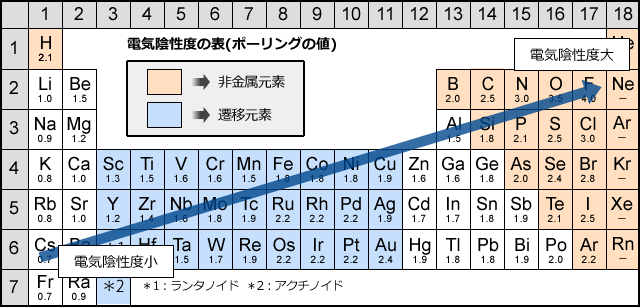
では、強さはどのようになっているかといいますと、
出典:http://blog.donaldo-plan.com/
周期表の右上に行くほど、
強くなる傾向にあります。
しかし、
ここで注意するのは、
18族の希ガスは
そもそも共有結合しないので、
電気陰性度の定義がないと
いうことです。
このような理由には、
「オクテット則」
という法則が関係しています。
「原子の最外殻電子の数が
8個あると化合物やイオンが
安定に存在するという経験則」
です。
これによって、
18族で最外殻電子が8個あり、
すでに安定な希ガスは、
わざわざ電子を出して
結合しようとしないのです。
逆に、
17族で最外殻電子が7個の
ハロゲンは
メチャメチャ電子が欲しいのです。
なので、
電気陰性度が最強の
原子界の横綱は、
F(フッ素)です。
次に、O(酸素)、
続いて、
N(窒素)とCl(塩素)
その次に、
C(炭素)、H(水素)となります。
問題を解くうえでは、
この順番が大切になってくるので、
この6つくらいは
覚えましょう。
覚え方は、
F>O>N,Cl>C>H
「フォン、狂っちゃう」
です。
これを使う例としては、
分子の極性などがあります。
極性は分子内の電気的な偏りです。
電気陰性度の差が大きいほど、
この偏りももでかくなります。
次の中で極性が最大のものを選べ。
H-C , H-F, H-O, H-Cl
という問題も、
電気陰性度の順番を知っていれば、
「横綱のFだから、H-F」
と即答できるのです。
他にも、
有機化学の分野では、
この電気の偏りがきっかけとなって
反応が起こったり、
酸性、塩基性がわかったりもします。
そのためにも、
まずここでは、
電気陰性度の大きさの順を
覚えておきましょう。
白紙を用意して、
何も見ずに、
電気陰性度を大きい順に6つ
書いてみましょう。
それでは今回はこれで。