酸の強さは何で決まる?
こんにちは、ナツキです!
前回は、酸と塩基について
説明しました。
今回はその「強さ」について、
考えていきましょう。
この強さを知っていると、
反応の進む向きや、有機化合物の分離、
できた塩が酸性なのか、塩基性なのか
などを考えられるようになります。
この話は、化学の得意な友達でも
おそらく知らないと思います。
苦手なあなたが、得意になるだけでなく、
得意な友達を追い越せるチャンスです!
先生や友達の発言、問題自体を、
いい意味で、
上から見れるようになるでしょう。
正直、友達の解答を、
「そんな大変な解き方でやってるの?」
と感じてしまいます。
テスト中にそう思えることの
安心感は半端じゃないです。
いわゆる裏技みたいなものです。
これができれば、
酸と塩基のことは、覚えずして、
考えてわかるようになります。
ぜひこのブログを読んでいる
あなただけに、
その裏技を紹介したいと思います。
さて、
酸の強さを話していく前に、
これから出てくる酸はすべて、
「ブレンステッドの酸」
と考えてください。
ブレンステッドの酸は、
「H+を与えるもの」でした。
つまり、
「どれだけH+を相手に与えたいか」
というのがが強さになります。
しかし、
「酸の強さ」を比べるためには、
与える相手を揃えないとなりません。
そこで、
相手をH2O(水)にして、
どれだけH+を与えるのかを
測定したものを、
「酸の解離定数」といいます
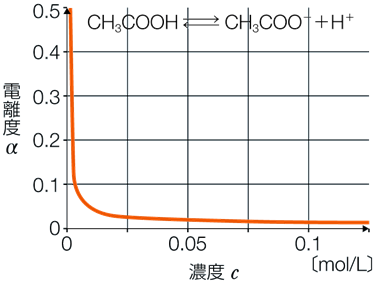
この解離定数Kaが大きいほど
強い酸ということになります。
この解離定数Kaは
強酸と呼ばれる塩酸(HCl)で、107
中くらいの酢酸(CH3COONa)で10−5
くらいです。
出典:http://sekatsu-kagaku.sub.jp/acid-base.htm
例えば、
塩酸はこのような反応式になります。
HCl + H2O → H3O+ + Cl–
この反応では、
HClが酸、H2Oが塩基として働きます。
では仮に、
逆(左←右)の反応が起こるとしたらどうでしょう。
右から左の反応が起こる場合、
H3O+ + Cl–→ HCl + H2O
このような反応式になります。
H+を与えるのがH3O+ で
受け取るのがCl–になるので、
H3O+が酸、Cl–が塩基となります。
酸のHClがH+を与えたのちに、
塩基となったこのCl–のことを、
HCl の「共役塩基」
と呼びます。
しかし、実際にはこの反応は起こりません。
強酸のHClは
メチャメチャH+をあげたいので、
その共役塩基のCl–は、
全然Hを受け取りたくないのです。
つまり、塩基としてのCl–は、
塩基として働かないレベルに、
めっちゃ弱いのです。
一般的に、逆の反応が起こるとすれば、
HA(酸)+H2O(塩基)
⇄
A- (共役塩基)+H3O+ (共役酸)
と書けます。
このとき、
酸が強いほど共役塩基は弱く、
塩基が強いほど、共役酸は弱いです。
とにかくこれが超重要です。
「塩が何性か求める問題」などでは、
この共役塩基の強さも
重要になってきます。
ですので、今回はまず、
元となる酸の強さの順
を覚えましょう。
「塩酸、硫酸、硝酸、水、
酢酸、炭酸、リン酸、フェノール」
あたりのKa(もしくはpKa)を調べて、
大きい順(pKaなら小さい順)に
並べてみましょう。
(もしかすると、化学図説に
のっているかも)
これは、有機化合物の分離や
反応式を作るうえでも、
重要になってくるので、
わかりやすくノートの見開きに
上から並べておくと、
調べるときに役立つでしょう。
次回は、これを使って、
実際に「塩が何性か」を
考えてみましょう。
それでは今回はこの辺で。





